Tuy nhiên, chúng tôi cũng đã phải đối mặt với những lời chỉ trích và thắc mắc từ một số quốc gia và công ty phương Tây, đặc biệt là những quốc gia đang phát triển vắc-xin của riêng họ, thường dựa trên các công nghệ chưa được chứng minh tính an toàn và hiệu quả. Cụ thể, những công nghệ này bao gồm các nền tảng mRNA và vector adenovirus của khỉ. Sau khi công bố kết quả của giai đoạn thử nghiệm lâm sàng đầu tiên và thứ hai đối với vắc-xin Sputnik V trên tạp chí y khoa The Lancet, ông Kirill Dmitriev CEO của RDIF xin tóm tắt câu trả lời cho những câu hỏi này, cũng như xin được đưa ra câu hỏi của mình.
Câu hỏi 1: Phải chăng các chuyên gia Nga đã sử dụng những dữ liệu khoa học đánh cắp để tạo vaccine?
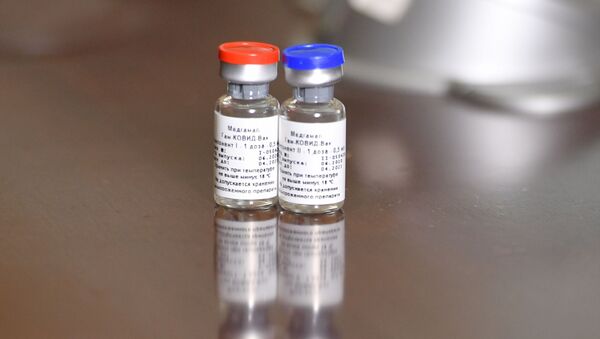
Tất nhiên là không phải thế, không ai trộm cắp gì cả. Vaccine sử dụng công nghệ hai vector độc đáo của adenovirus ở người, mà thời điểm hiện tại trên thế giới chưa ai có. Các vector là virus nhân tạo, không có khả năng sao chép, chúng mang trong mình vật liệu di truyền từ «gai» coronavirus. Công nghệ của chúng tôi sử dụng hai vector siêu vi adenovirus khác nhau ở người, Ad5 và Ad26, để tiêm lần đầu và lần thứ hai. Đối với việc tiêm vắc-xin ngừa coronavirus, Nga đã sửa đổi thành công nền tảng hai vector hiện có được phát triển vào năm 2015 để chống lại bệnh sốt Ebola, đã trải qua tất cả các giai đoạn nghiên cứu lâm sàng và giúp đánh bại dịch bệnh Ebola ở châu Phi vào năm 2017.
Rõ ràng, sau những ồn ào ban đầu xung quanh vấn đề này, ngay cả những người chỉ trích Nga gay gắt nhất cũng nhanh chóng quên đi do tính chất vô căn cứ của nó, tuy nhiên, chúng tôi cho rằng quan trọng là nhắc lại điều này, được coi là nỗ lực bôi nhọ vắc-xin Nga ngay cả trước khi nó được đăng ký.
Câu hỏi 2: Khi nào công bố kết quả thử nghiệm lâm sàng giai đoạn I và II?
Những kết quả này đã được công bố trên tạp chí The Lancet ngày 4 tháng 9, một trong những ấn phẩm y học lâu đời nhất và uy tín nhất thế giới. Đó mới chỉ là khởi đầu của một loạt bài đăng về vắc-xin. Các điểm then chốt của bài báo là như sau:
- Thử nghiệm lâm sàng giai đoạn I-II của Sputnik V cho thấy không gây tác dụng phụ nghiêm trọng theo bất kỳ tiêu chí nào, trong khi tần suất tác dụng phụ nghiêm trọng của hàng loạt vaccine nước ngoài (của AstraZeneca, Pfitzer, BioNtech, Novavax và CanSino) dao động từ 1 đến 25%.
- Ở 100% thành viên tham gia thử nghiệm lâm sàng, Sputnik V đã tạo ra phản hồi miễn dịch ổn định. Mức độ kháng thể trung hòa virus ở các tình nguyện viên được tiêm Sputnik V cao hơn 1,5 lần so với những bệnh nhân từng mắc bệnh và hồi phục. Ngược lại, sau khi thử nghiệm lâm sàng loại vaccine của công ty dược phẩm Anh AstraZeneca thì mức độ kháng thể ở những người tình nguyện tiêm gần như tương đương với mức kháng thể ở những người đã mắc coronavirus rồi khỏi bệnh. Cũng cần lưu ý rằng, trong quá trình thử nghiệm lâm sàng đối với vắc-xin Sputnik V, tất cả các tình nguyện viên đều phát triển khả năng miễn dịch tế bào T, đại diện là tế bào CD4+ và CD8+. Các tế bào này đảm bảo nhận biết và tiêu diệt các tế bào bị nhiễm SARS-CoV-2, tạo cơ sở hình thành khả năng miễn dịch lâu dài.
- Các chuyên gia của Trung tâm Nghiên cứu Dịch tễ và Vi sinh Quốc gia mang tên Gamaleya đã có thể chứng minh tính hiệu quả của nền tảng vector adenovirus ở người, bất kể e ngại rằng trong cơ thể những cá nhân được tiêm chủng có thể đã sẵn có khả năng miễn dịch với adenovirus của người. Đã xác định được liều lượng an toàn tối ưu của vaccine, đảm bảo để trong quá trình thử nghiệm 100% số người tiêm chủng đều đạt mức miễn dịch cần thiết. Những lo ngại về khả năng miễn dịch đã hình thành từ trước đối với các căn bệnh truyền nhiễm adenovirus là một trong những lý do chính dẫn đến sự xuất hiện của các phương pháp thay thế như những nền tảng dựa trên vector adenovirus của khỉ hoặc mRNA, vốn chưa được nghiên cứu và thử nghiệm trong thời gian dài nhiều năm. Hiệu quả đã được chứng minh của Sputnik V khiến việc đẩy nhanh quá trình phát triển vắc-xin dựa trên các nền tảng chưa được kiểm chứng, tiềm ẩn nguy cơ không an toàn và có thể gây hại cho sức khỏe, trở nên ít cấp thiết hơn.
- Nhờ cách sử dụng hai vector khác nhau trên cơ sở hai loại adenovirus ở người là Ad5 và Ad26 trong hai lần tiêm cách biệt, có thể đạt được phản hồi miễn dịch hiệu quả cao hơn. Trong khi đó, với trường hợp chỉ sử dụng cùng một vector, hệ thống miễn dịch tự thân sẽ kích hoạt cơ chế bảo vệ và có thể từ chối vaccine khi tiêm lặp lại. Do đó, việc sử dụng hai vectơ khác nhau trong vắc-xin Sputnik V giúp tránh được tác dụng trung hòa có thể xảy ra và tạo ra khả năng miễn dịch mạnh hơn và lâu dài hơn.
Câu hỏi 3: Liệu số tình nguyện viên trong thử nghiệm lâm sàng giai đoạn đầu và giai đoạn hai có quá ít hay không?
Ở cấp độ bề ngoài, thử nghiệm vaccine Sputnik V với 76 tình nguyện viên có vẻ khiêm tốn hơn về phạm vi, so với thử nghiệm vắc xin AstraZeneca trên 1.077 người. Tuy nhiên, thiết kế thử nghiệm Sputnik V hiệu quả hơn và dựa trên các giả thiết khoa học đúng đắn. Ban đầu, AstraZeneca chỉ tiến hành thử nghiệm với một lần tiêm, nhưng hóa ra đây là giả thiết sai lầm, vì chỉ có mẫu tiêm hai lần mới cho phép tạo ra miễn dịch lâu dài. Công ty đã thừa nhận điều này sau khi thử nghiệm. Do hậu quả của các giả thiết sai lầm này, AstraZeneca đã thử nghiệm mẫu hai lần tiêm chỉ với 10 người trong số 1.077 người. Như vậy, tổng số người được tiêm hai mũi vaccine Sputnik V trong giai đoạn đầu và giai đoạn hai của thử nghiệm lâm sàng nhiều gấp bốn lần so với số người được tiêm hai mũi vắc-xin AstraZeneca. Tuy nhiên, hầu hết các phương tiện truyền thông đã bỏ qua chuyện này.
Câu hỏi 4: Vaccine Nga có được thử nghiệm lâm sàng với nhiều người hay không?
Các nghiên cứu hậu đăng ký với hơn 40.000 người tham gia đã được tiến hành ở Nga vào ngày 26 tháng 8, thậm chí trước cả khi AstraZeneca Anh-Thụy Điển bắt đầu thử nghiệm giai đoạn III đối với vaccine của họ ở Hoa Kỳ với 30.000 người tham gia. Các cuộc thử nghiệm lâm sàng của vaccine Sputnik V ở Saudi Arabia, Các Tiểu vương quốc Ả Rập Thống nhất, Philippines, Ấn Độ và Brazil sẽ được thực hiện trong tháng này. Kết quả sơ bộ sẽ được công bố vào tháng 10-11 năm 2020.
Câu hỏi 5: Tại sao Sputnik V lại được đăng ký nhanh chóng như vậy?
Việc đăng ký được thực hiện theo quy trình rút gọn nhờ vào kết quả tích cực của giai đoạn thử nghiệm lâm sàng đầu tiên và giai đoạn thứ hai, đồng thời căn cứ vào thực tế là nền tảng dựa trên vectơ virus gây bệnh ở người đã được xác nhận là nền tảng an toàn nhất trên thế giới trong nhiều thập kỷ nghiên cứu, bao gồm 75 bài đăng trên các tạp chí khoa học quốc tế và hơn 250 thử nghiệm lâm sàng.
Các nhà khoa học Nga đã trình bày toàn bộ dữ liệu có sức thuyết phục về tính chất an toàn của việc sử dụng vaccine adenovirus cho người, dựa trên cơ sở các nghiên cứu được thực hiện ở các nước khác nhau ngay từ năm 1953. Theo số liệu này, kể từ năm 1971, hơn 10 triệu quân nhân Hoa Kỳ đã được tiêm vắc-xin trên nền tảng adenovirus ở người. Thuốc trị ung thư Gendicine, dựa trên các vector adenovirus ở người, đã được sử dụng để điều trị cho hơn 30.000 bệnh nhân ở Trung Quốc trong 15 năm. Hơn 25.000 người trên toàn thế giới đã tham gia vào các thử nghiệm lâm sàng về vắc-xin dựa trên công nghệ vectơ adenovirus ở người sử dụng các vectơ tương tự như trong vắc-xin Sputnik V. Kể từ năm 2015, hơn 3 nghìn người đã được tiêm vắc-xin ngừa Ebola và vắc-xin ngừa Hội chứng hô hấp cấp Trung Đông (MERS) được tạo ra tại Trung tâm nghiên cứu quốc gia về dịch tễ học và vi sinh vật mang tên Gamaleya dựa trên vector adenovirus ở người.
Vắc-xin đã được đăng ký tại Nga, vì nó dựa trên nền tảng của các vectơ adenovirus ở người, vốn đã được chứng minh từ trước đây là an toàn và hiệu quả. Sau khi Sputnik V đăng ký ở Nga, các quốc gia khác cũng công bố kế hoạch tăng tốc đăng ký vaccine để sử dụng trong trường hợp khẩn cấp. Vaccine của Sinovac Biotech đã nhận được chấp thuận tương tự ở Trung Quốc. Chính phủ Anh và ông Stephen Hahn đứng đầu Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cũng tuyên bố về khả năng cấp tốc đăng ký vaccine của Anh và Hoa Kỳ, bất kể những phản đối gay gắt trước đó.
Câu hỏi 6: Có ai đó sử dụng công nghệ tương tự để sản xuất vắc xin hay không?
Một số công ty khác đang sử dụng các nền tảng dựa trên vectơ adenoviral ở người để chế tạo vaccine ngừa coronavirus. Ví dụ, Johnson & Johnson chỉ sử dụng vector huyết thanh thứ 26, trong khi công ty CanSino của Trung Quốc sử dụng vector huyết thanh thứ 5. Vắc xin Sputnik V sử dụng cả hai vector này. Công trình của Johnson & Johnson và CanSino không chỉ khẳng định giá trị của phương pháp tiếp cận của Nga, mà còn chứng minh tính ưu việt của vắc xin Sputnik V, vì các nghiên cứu đã chỉ ra rằng sử dụng hai vector cho kết quả tốt hơn so với sử dụng một vector.
Câu hỏi của chúng tôi
Theo tất cả những gì được nói đến ở trên, với tư cách rõ ràng và được công nhận là nước đi đầu trong việc tạo ra vắc-xin và là nước đã tạo ra loại vắc-xin an toàn và hiệu quả nhất chống lại coronavirus, Nga cũng muốn đặt câu hỏi cho các nhà phát triển vắc-xin phương Tây, những nơi sử dụng nền tảng dựa trên vectơ adenovirus hoặc mRNA của khỉ. Bây giờ chúng tôi muốn hỏi những người chỉ trích: "Tại sao các vị nhìn thấy bụi trong mắt người anh em của mình mà lại không nhìn thấy dằm trong mắt mình?"
- Câu hỏi 1: Các vị đã tiến hành các nghiên cứu trong thời gian dài về nguy cơ nảy sinh các loại bệnh ung thư và ảnh hưởng của các công nghệ dựa trên vectơ mRNA và adenovirus của khỉ đến khả năng sinh sản chưa? (Gợi ý: chưa)
- Câu hỏi 2: Liệu có phải chính vì chưa có những nghiên cứu như vậy nên một số công ty dược phẩm hàng đầu phát triển vắc-xin dựa trên các công nghệ này đang đàm phán với các quốc gia mua vắc-xin những điều khoản để bảo vệ họ tránh khỏi những hậu quả pháp lý, trong trường hợp có những tác dụng nghiêm trọng không lường trước được?
- Câu hỏi 3: Tại sao các phương tiện truyền thông phương Tây không đưa tin về việc không có những nghiên cứu trong thời gian dài đối với vắc-xin phát triển dựa trên công nghệ mRNA và công nghệ vector adenovirus của khỉ?
Vắc xin dành cho con người hay vắc-xin của khỉ
Các vắc-xin dựa trên công nghệ mRNA và vectơ adenoviral của khỉ chưa từng được sử dụng trước đây và chưa bao giờ được các cơ quan quản lý chấp thuận. Nghiên cứu về tính hiệu quả của chúng chậm hơn nghiên cứu tương tự trên các nền tảng vector adenoviral ở người ít nhất 20 năm. Tuy nhiên, các nhà sản xuất đã có hợp đồng hàng tỷ đô la từ chính phủ các nước phương Tây và có thể đăng ký nhanh, sau khi đã bảo vệ bản thân khỏi những hậu quả pháp lý tiềm ẩn. Loại vắc-xin dựa trên công nghệ mRNA có nhiều ưu điểm, những ưu điểm đó có thể đóng vai trò quan trọng trong tương lai, nhưng chúng chưa được chứng minh về tính an toàn trên bình diện lâu dài.
Chúng tôi cho rằng cần phải nói cho mọi người biết về những rủi ro khi phê duyệt các giải pháp mới chưa được kiểm chứng, chẳng hạn như nền tảng mRNA và vector adenovirus của khỉ. Chúng tôi đánh giá rất cao ý định của các công ty dược phẩm phương Tây trong việc công bố cái gọi là "bản tuyên ngôn an toàn" trong thời gian tới. Đồng thời, chúng tôi hy vọng rằng tuyên ngôn như vậy áp dụng không chỉ riêng đối với các kết quả thử nghiệm lâm sàng ngắn hạn, mà còn có thể đảm bảo sẽ không có rủi ro đáng kể về lâu dài liên quan đến các bệnh ung thư và việc ảnh hưởng đến khả năng sinh sản do các loại vắc-xin này gây ra. Thông tin đó sẽ giúp bảo vệ sức khỏe con người và giúp thế giới lập kế hoạch dài hạn.
Không phải tất cả các loại vác xin đều được tạo ra như nhau
Tóm lại, cần lưu ý rằng vắc-xin có các nền tảng khác nhau. Sputnik V được xây dựng trên nền tảng an toàn nhất và đã được chứng minh, nó được đăng ký để sử dụng trong những trường hợp khẩn cấp, tuân thủ đầy đủ tất cả các quy trình và luật lệ của Nga. Một số cơ quan quản lý ở phương Tây cũng đang xem xét xúc tiến việc đăng ký thuốc để sử dụng trong trường hợp khẩn cấp, nhưng lần này là đối với vắc-xin được tạo ra trên cơ sở công nghệ mới chưa được thử nghiệm.
Chúng tôi hy vọng rằng các câu hỏi của chúng tôi về những rủi ro dài hạn sẽ được giải đáp cũng như bất kỳ câu hỏi nào khác về các nền tảng vắc-xin chưa được thử nghiệm có thể phát sinh trong tương lai. Đại dịch tồi tệ nhất trong hàng trăm năm nay đã buộc tất cả chúng ta phải tìm kiếm các giải pháp. Nhưng chúng tôi hy vọng những người chỉ trích chúng tôi sẽ đáp ứng các tiêu chuẩn nghiêm ngặt về tính an toàn và minh bạch, mà họ đã tuân thủ khi chỉ trích vắc-xin của Nga. Dù thế nào đi nữa, chúng ta phải cùng nhau chống lại đại dịch, bỏ qua mọi định kiến, và trong điều kiện hoàn toàn minh bạch và tin cậy lẫn nhau.
Đọc thêm: