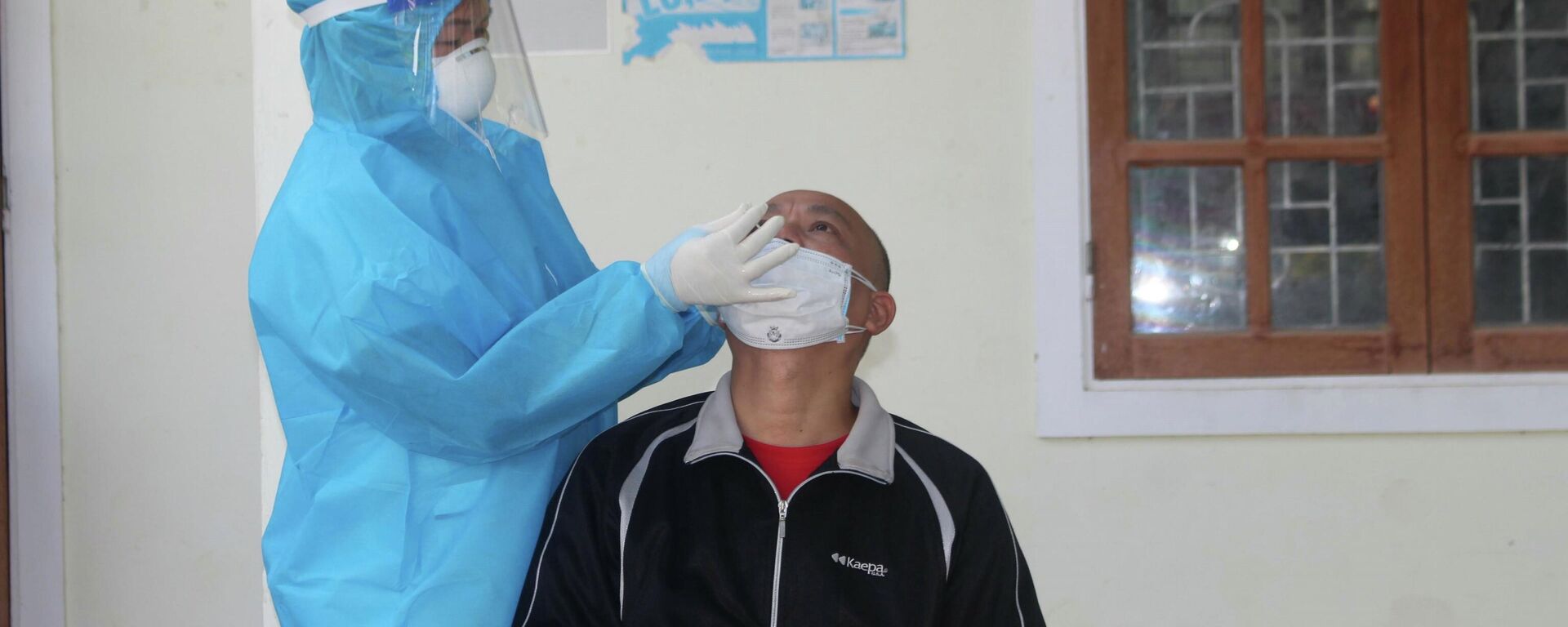
Ai mới là chủ thực sự của Công ty Việt Á?
17:51 22.12.2021 (Đã cập nhật: 18:10 22.12.2021)
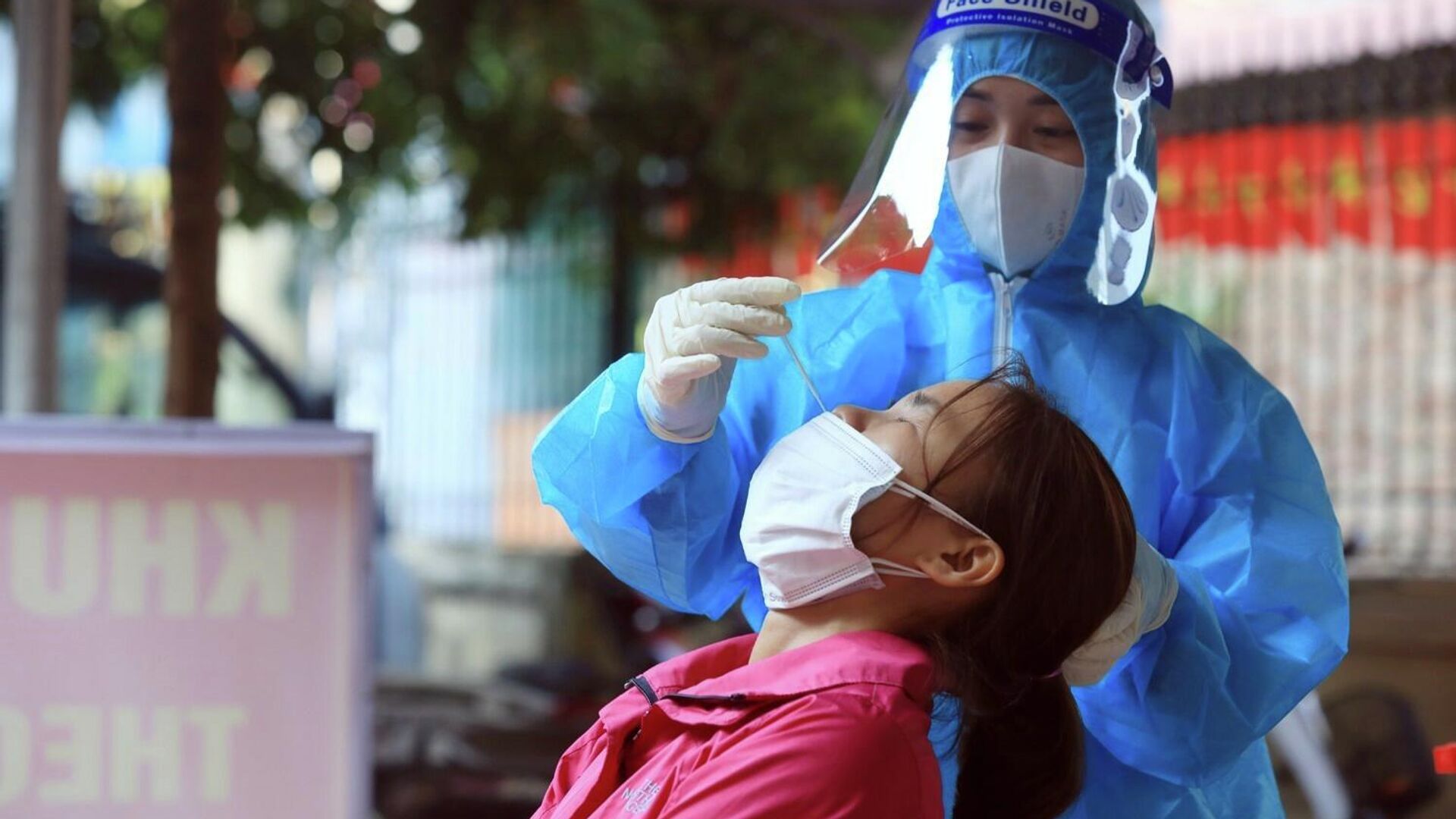
© Ảnh : Tuấn Anh - TTXVN
Đăng ký
Dư luận đề nghị làm rõ ai mới là chủ thực sự của Công ty Việt Á, có hay không việc đi đêm, móc nối, hối lộ. Ai ‘bảo kê’, bao che để Việt Á vô tư nâng khống giá thiết bị trong suốt thời gian dài trước khi Bộ Công an bắt Phan Quốc Việt, Phạm Duy Tuyến?
Chuyên gia nêu rõ, vụ nâng khống giá kit test xét nghiệm của Phan Quốc Việt và Công ty Việt Á rần rần như thế mà lãnh đạo bảo “không biết” thì ai chấp nhận được? Sau đó không chỉ là “một, hai nhân vật”, mà còn rất nhiều “dây dợ” liên quan.
Cùng với đó, Trưởng Đại diện Tổ chức Y tế Thế giới tại Việt Nam TS. Kidong Park cũng vừa trả lời vì sao WHO không chấp thuận bộ kit test xét nghiệm Covid-19 của Công ty Việt Á.
Vì sao WHO không chấp thuận kit test của Công ty Việt Á?
Theo TS. Kidong Park, hồ sơ sản phẩm kit test virus SARS-CoV-2 của Việt Nam (Công ty Việt Á) đã được WHO kiểm nghiệm, đánh giá, nhưng không đáp ứng được các yêu cầu về an toàn, công năng và/hoặc QMS để đủ tiêu chuẩn được thông qua.
Như Sputnik đã thông tin, Công ty Việt Á do Phan Quốc Việt thành lập, giữ chức Chủ tịch Hội đồng quản trị kiêm Tổng Giám đốc, người đại diện pháp luật. Tháng 4/2020, Công ty Việt Á được Bộ Y tế Việt Nam cấp phép đăng ký lưu hành cho sản phẩm “Kit xét nghiệm Covid-19”.
Bộ kit test của Công ty Việt Á được cấp phép rất nhanh chóng trong tình hình dịch bệnh khẩn cấp tại Việt Nam. Từ ngày 5/3/2020, Bộ Khoa học và Công nghệ đã họp báo công bố kết quả nghiên cứu chế tạo bộ sinh phẩm Real-time RT-PCR phát hiện virus corona chủng mới SARS-CoV-2 do Học viện Quân y chủ trì, phối hợp với Công ty CP Việt Á thực hiện.
Phía Công ty Việt Á khẳng định, bộ kit test của Việt Nam được thí nghiệm kiểm định tiêu chí độ nhạy, độ đặc hiệu, độ chính xác, độ lặp lại thực hiện tại labo chuẩn thức của Việt Á và Học viện Quân y. Đặc biệt, kết quả nghiên cứu tiến hành cho thấy “bộ kit ‘made in Vietnam’ này đáp ứng tiêu chí tương đương bộ sinh phẩm do US CDC và WHO sản xuất”.
Công ty Việt Á còn cho biết, Bộ Y tế và Chăm sóc xã hội Anh đã cấp giấy chứng nhận đạt tiêu chuẩn châu Âu (CE) và cấp giấy chứng nhận lưu hành tự do (CFS) cho bộ sản phẩm xét nghiệm Covid-19 do Bộ Khoa học và Công nghệ giao Học viện Quân y cùng Công ty Việt Á phối hợp nghiên cứu, sản xuất.
Sau đó, Công ty Việt Á còn thông tin bộ kit test xét nghiệm của Việt Á mang mã hiệu LightPower iVASARS-CoV-2 1stRT-rPCR Kit được WHO chấp thuận với mã số EUL 0524‐210‐00.
Tuy nhiên, Tổ chức Y tế Thế giới chưa chấp nhận sản phẩm này của Việt Nam. Tại báo cáo công khai về đánh giá sử dụng khẩn cấp của WHO hôm 20/10/2020, kết quả thẩm định của Tổ chức Y tế Thế giới với bộ xét nghiệm Covid-19 của Việt Á là “Not Accepted” (tức Không được chấp nhận). WHO cho rằng, bộ kit test xét nghiệm LightPower iVASARS-CoV-2 1stRT-rPCR Kit với mã VA. A02-055H, do Công ty Cổ phần Công nghệ Việt Á, địa chỉ 372A/8 Hồ Văn Huê, phường 9, quận Phú Nhuận, TP.HCM, Việt Nam sản xuất “không đủ điều kiện” để vào chương trình mua sắm (vật tư y tế) của WHO.
Hồi 9/6/2021 vừa qua, WHO tiếp tục công bố danh mục các sản phẩm không được chấp nhận theo quy trình đánh giá sử dụng khẩn cấp với lưu ý các hồ sơ đã được đánh giá và không cung cấp được bằng chứng, dữ liệu, tài liệu cần thiết về độ an toàn, hiệu quả, hoặc hệ thống quản lý chất lượng (QMS). Trong danh sách này, ở hạng mục test (xét nghiệm) virus SARS-CoV-2 có nêu bộ kit của Việt Nam là LightPower iVASARS-CoV-2 1stRT-rPCR Kit, mã số sản phẩm VA. A02-055H, số hồ sơ đăng ký EUL 0524-210-00 tiếp tục không được chấp nhận.
Lý giải về vấn đề này, TS. Kidong Park, Trưởng Đại diện Tổ chức Y tế Thế giới tại Việt Nam cho biết, có một sản phẩm kit test PCR Covid-19 do Công ty Việt Á sản xuất đã nộp hồ sơ cho chẩn đoán in vitro (IVD) Covid-19 để WHO đưa vào Danh sách sử dụng khẩn cấp (EUL).
Tên gọi của sản phẩm trong hồ sơ là LightPower iVASARS-CoV-2 1stRT-rPCR Kit. Sản phẩm của Công ty Việt Á có mã hồ sơ đăng ký EUL là "EUL 0524-210-00".
“Tuy nhiên, qua quá trình kiểm tra, đánh giá, hồ sơ sản phẩm này không đáp ứng được các yêu cầu về an toàn, công năng và/hoặc QMS (tức Hệ thống quản lý chất lượng thiết bị y tế)”, Trưởng Đại diện WHO tại Việt Nam khẳng định.
TS. Kidong Park cũng lưu ý, Danh sách EUL của WHO không phải là danh sách đầy đủ các sản phẩm IVD được sử dụng trong chẩn đoán Covid-19.
Lý giải về quy trình thiết lập Danh sách sử dụng khẩn cấp (EUL) trong chẩn đoán in vitro (IVD) bệnh Covid-19, Trưởng đại diện WHO tại Việt Nam cho biết, Tổ chức Y tế Thế giới có cơ chế tiền kiểm (PQ) nhằm đánh giá tính an toàn, chất lượng và hiệu quả của các sản phẩm y tế thiết yếu.
Theo ông Kidong Park khẳng định trong cuộc phỏng vấn với NLĐ, cơ chế tiền kiểm của WHO sẽ đánh giá các sản phẩm gồm chẩn đoán in vitro (IVD), thiết bị cắt bao quy đầu cho nam giới, thuốc, vaccine, thiết bị dùng trong tiêm chủng và thiết bị trong dây chuyền lạnh, cũng như sản phẩm kiểm soát vector.
Mục tiêu của Cơ chế tiền kiểm là nhằm đảm bảo các sản phẩm y tế thiết yếu phải đáp ứng các tiêu chuẩn toàn cầu về chất lượng, an toàn và hiệu quả, từ đó tối ưu hóa việc sử dụng các nguồn lực y tế và cải thiện sức khỏe.
Công tác tiền kiểm được thực hiện một cách minh bạch, khoa học, trải qua các bước từ xem xét hồ sơ, thử nghiệm sản phẩm, đánh giá công năng cho đến kiểm tra công tác tổ chức nghiên cứu của cơ sở sản xuất.
“Kết quả của PQ bao gồm danh sách các sản phẩm đã được tiền kiểm, danh sách các phòng xét nghiệm đã được tiền kiểm chất lượng và các Báo cáo Kiểm tra và Đánh giá công khai của WHO. Kết quả này được Liên Hiệp Quốc và các cơ sở cung ứng khác sử dụng trong quyết định mua bán các sản phẩm y tế”, TS. Kidong Park nêu rõ.
Quy trình EUL được phát triển nhằm tận dụng sự sẵn có của các sản phẩm y tế sử dụng trong các tình huống khẩn cấp y tế công cộng.
EUL hỗ trợ các cơ sở cung ứng và các quốc gia thành viên có quyết định phù hợp khi sử dụng một IVD cụ thể, dựa trên các dữ liệu tối thiểu về chất lượng, an toàn và công năng.
Theo ông Park, việc đảm bảo chất lượng, an toàn và công năng của IVD là một phần quan trọng trong chiến lược tổng thể nhằm kiểm soát đại dịch Covid-19.
Cũng theo TS. Kidong Park, tính đến ngày 20/12/2021, đã có 28 sản phẩm IVD Covid-19 được chấp thuận thông qua quy trình EUL của WHO.
Đồng thời, có 46 sản phẩm IVD khác không đáp ứng được các hồ sơ cần thiết về an toàn, công năng và / hoặc hệ thống quản lý chất lượng (QMS); các hồ sơ này đã bị rút lại hoặc không đáp ứng các tiêu chí đánh giá của EUL.
“Sai sót” và “đúng quy trình”
Liên quan đến vụ thổi giá kit test của Công ty Việt Á cũng như việc bắt giữ Phan Quốc Việt và đồng phạm, xuất hiện dấu hỏi rất lớn liên quan đến trách nhiệm các bên liên quan.
Bộ Y tế cho rằng, việc cấp phép cho kit test của Công ty Việt Á là “căn cứ theo đề xuất của Bộ Khoa học và Công nghệ”. Vậy trách nhiệm rốt cuộc thuộc về Bộ nào?
Trong thông cáo báo chí phát đi hôm 21/12, Bộ Y tế khẳng định, đã làm đúng quy trình, “thực hiện đúng quy định” trong trong cấp phép lưu hành sinh phẩm xét nghiệm của Công ty cổ phần Công nghệ Việt Á”.
Theo Bộ Y tế, 3/3/2020, Hội đồng Khoa học – Công nghệ cấp Quốc gia do Bộ trưởng Bộ Khoa học và Công nghệ thành lập đã họp, đánh giá kết quả nghiên cứu chế tạo bộ kit real-time RT-PCR one step của Học viện Quân y và Công ty cổ phần công nghệ Việt Á phối hợp nghiên cứu, sản xuất.
Sau khi xem xét, 8 thành viên của Hội đồng thống nhất thông qua và chuyển hồ sơ kiến nghị Bộ Y tế cấp phép sử dụng đối với bộ kit test trên. Trên cơ sở đó, ngày 4/3/2020, Bộ Y tế ban hành Quyết định 774 về ban hành danh mục 2 sinh phẩm chẩn đoán in vitro xét nghiệm virus corona (SARS-CoV-2) được cấp số đăng ký do Học viện Quân y và Công ty cổ phần công nghệ Việt Á sản xuất để phục vụ kịp thời công tác phòng, chống dịch Covid-19.
Bộ Y tế nêu rõ, việc cấp phép căn cứ vào ý kiến của Hội đồng đánh giá, nghiệm thu kết quả giai đoạn 1 đề tài độc lập cấp quốc gia đột xuất phòng chống dịch bệnh viêm đường hô hấp cấp do chủng mới của virus corona. Đây là kết quả của nhiệm vụ khoa học và công nghệ cấp quốc gia do Bộ Khoa học và Công nghệ phê duyệt, được thực hiện giữa Học viện Quân y và Công ty cổ phần Công nghệ Việt Á.
Đồng thời, theo kết quả đánh giá đáp ứng về độ nhạy và độ đặc hiệu của Viện Vệ sinh dịch tễ Trung ương, kết quả xác nhận cơ sở sản xuất của Công ty Việt Á đã đạt tiêu chuẩn ISO 13485:2016. Tính đến 20/12/2021, Bộ Y tế đã cấp phép cho 146 sinh phẩm xét nghiệm SARS-CoV-2, trong đó có 46 sinh phẩm xét nghiệm vật liệu di truyền (PCR, LAMP).
“Tất cả các sản phẩm cấp phép đều đã được đánh giá đạt yêu cầu, đáp ứng tiêu chuẩn, chất lượng của Việt Nam và đảm bảo đúng theo các quy định hiện hành. Các sản phẩm sau khi được cấp phép đều được theo dõi chất lượng và tính ổn định”, Bộ Y tế khẳng định.
Bộ Y tế cũng nhấn mạnh, cấp phép của Bộ Y tế đối với sản phẩm của Công ty cổ phần Công nghệ Việt Á và các nhà sản xuất khác không phụ thuộc vào danh sách do WHO công bố. Giá sinh phẩm xét nghiệm (như trong trường hợp của Việt Á – PV) cũng phải thông qua đấu thầu công khai, minh bạch. Đồng thời, Bộ Y tế đã cương quyết phòng chống tiêu cực, tham nhũng trong mua sắm, đấu thầu, còn các địa phương phải thực hiện việc đấu thầu mua sắm theo các quy định hiện hành của Nhà nước và tự chịu trách nhiệm về việc mua sắm của mình.
Trong khi đó, Bộ Khoa học và Công nghệ “nhận sai sót” liên quan đến việc cấp phép cho bộ kit test của Công ty Việt Á. Theo đó, hôm 21/12, ông Trịnh Thanh Hùng, Phó Vụ trưởng Vụ Khoa học và Công nghệ các khối ngành Kinh tế - Kỹ thuật, Bộ Khoa học và Công nghệ, thừa nhận Bộ này chưa xem xét kỹ lưỡng thông tin phản hồi của WHO về bộ kit test của Công ty Việt Á.
“Đúng là WHO mới chỉ “chấp thuận đưa kit test này vào quy trình đánh giá xem xét sử dụng” chứ không phải “đã chấp nhận để sử dụng”. Đây là sơ suất của Bộ Khoa học và Công nghệ”, ông Hùng nói.
Bộ Khoa học và Công nghệ cũng đã gỡ thông tin đăng tải công bố đánh giá của WHO và Bộ Y tế Anh cấp chứng nhận đạt chuẩn châu Âu cho bộ kit test của Công ty Việt Á.
Dư luận đặt câu hỏi, trước khi Bộ Công an khởi tố vụ án của Công ty Việt Á, khởi tố Phan Quốc Việt, Phạm Duy Tuyến – Giám đốc CDC Hải Dương (đã nhận 30 tỷ đồng lại quả, biếu tặng) thì các Bộ Y tế, Bộ Khoa học và Công nghệ có nắm được hay không.
Riêng về cá nhân ông Phạm Duy Tuyến, Ủy ban Kiểm tra Đảng ủy Khối các cơ quan tỉnh Hải Dương đã quyết định đình chỉ sinh hoạt đảng đối với ông Phạm Duy Tuyến, Đảng ủy viên Đảng bộ Sở Y tế, Bí thư Chi bộ CDC Hải Dương ngay trong ngày 21/12.
Cùng ngày, Giám đốc Sở Y tế tỉnh Hải Dương đã ký quyết định tạm đình chỉ công tác đối với ông Phạm Duy Tuyến.
Tại Hội nghị lần thứ 48 của Ban Thường vụ Tỉnh ủy Hải Dương cùng ngày, Bí thư Tỉnh ủy Hải Dương Phạm Xuân Thăng đã đề nghị các cơ quan chức năng khẩn trương kiểm tra dấu hiệu vi phạm và xử lý theo quy định đối với Giám đốc CDC Hải Dương.
Phải làm rõ ai chống lưng, “bảo kê” cho Công ty Việt Á
Như Sputnik Việt Nam đã đề cập, phát biểu tại phiên họp thứ 6, đợt 2 của Ủy ban Thường vụ Quốc hội, Chủ nhiệm Ủy ban Pháp luật Hoàng Thanh Tùng đề nghị làm rõ trách nhiệm, kể các của các Bộ, để xử nghiêm vụ việc mà “dư luận đặc biệt quan tâm” là vụ nâng khống giá kit test của Việt Á.

Chủ nhiệm Ủy ban Pháp luật của Quốc hội Hoàng Thanh Tùng trình bày báo cáo
© Ảnh : Phạm Kiên - TTXVN
“Ở rất nhiều địa phương, kết quả đấu thầu giá kit xét nghiệm của Công ty Việt Á cũng rất cao, trên dưới 500.000 đồng/kit, trong khi tại thời điểm báo chí phản ánh “loạn giá kit xét nghiệm” đã đề cập đến việc nếu mua của nước ngoài số lượng lớn có khi chỉ 1-2 USD/kit xét nghiệm”, ông Tùng so sánh.
Nói đâu xa, chỉ riêng một mình ông Phạm Duy Tuyến của CDC Hải Dương đã nhận đến gần 30 tỷ đồng tiền “lại quả” từ Phan Quốc Việt theo điều tra của Bộ Công an, trong khi đó, bộ kit test này được cho là đã cung ứng bộ kit xét nghiệm Covid-19 này cho Trung tâm Kiểm soát bệnh tật (CDC) và các cơ sở y tế khác của 62 tỉnh, thành phố trên cả nước với doanh thu khoảng gần 4.000 tỷ đồng.
Theo ông Lê Như Tiến, ĐBQH khóa XIII, rõ ràng, tình trạng thông thầu, nâng giá thiết bị, vật tư y tế đã được đề cập nhiều trong thời gian qua. Nhiều cán bộ quản lý trong ngành y tế, ngay cả cấp thứ trưởng cũng đã bị khởi tố, điều tra.
“Đây là điều đáng báo động đối với ngành y tế”, ông Tiến lưu ý.
Đối với vụ án của Công ty Việt Á, theo ông Tiến, Phan Quốc Việt không thể một mình nâng giá kit xét nghiệm Covid-19 như thế được. Do vậy, nếu phát hiện ai trong cơ quan nhà nước “chống lưng”, hay “bảo kê” cho việc này phải xử lý nghiêm. Trao đổi với TPO, ông Tiến nhấn mạnh, chính đồng tiền đã làm cho con người không còn giữ được phẩm giá. Các đối tượng đã lợi dụng dịch bệnh, làm mọi giá để kiếm tiền, điều đó không thể chấp nhận.
Chuyên gia đặt vấn đề, cần làm rõ trách nhiệm, cần xem xét công tác thanh tra, kiểm tra ngành y tế liệu đã phát huy hết vai trò hay chưa.
“Không rõ cơ chế quản lý của ngành y tế như thế nào mà lại để xảy ra nhiều vụ việc đáng tiếc đến như vậy? Ngoài trách nhiệm của Bộ Y tế, cần xem xét vai trò, trách nhiệm của các cấp, ngành từ Trung ương đến địa phương. Để xử lý tận gốc vấn đề phải có hình thức kỷ luật thật nghiêm khắc đối với những tổ chức, cá nhân có liên quan”, ông Lê Như Tiến khẳng định.
Ai mới là chủ thực sự của Công ty Việt Á?
TS. Lưu Bình Nhưỡng, Đại biểu Quốc hội khóa XIV, lưu ý đến tình trạng buông lỏng quản lý.
Theo ông Nhưỡng, không thể nói rằng, cấp dưới của mình làm chuyện gì mà cấp trên lại không biết, điều này rất vô lý.
“Làm gì có chuyện trong cùng ngành y tế mà quân của mình làm gì mình lại không nắm được, không ai có thể chấp nhận điều đó. Tôi cho rằng, vị nào phát ngôn rằng, không biết đến chuyện mua bán của CDC Hải Dương diễn ra như thế nào là thể hiện người đó đang vô trách nhiệm với những sự gì đang xảy ra”, TS. Lưu Bình Nhưỡng nói.
Theo ông Nhưỡng, cơ quan quản lý mà lại buông lỏng quản lý để xảy ra sai sót trong lúc xét duyệt hồ sơ thì không thể chấp nhận được. Trong khi trước đó, đã có nhiều vụ nâng khống giá vật tư y tế liên quan đến CDC của một số địa phương đã bị cơ quan điều tra phanh phui. Tức hoạt động của các CDC tại địa phương còn lại kiểu gì cũng sẽ nằm trong “tầm ngắm”, vậy tại sao Sở Y tế Hải Dương lại không nắm được, quản lý được. Khẳng định với GDVN, TS. Lưu Bình Nhưỡng cho rằng, dư luận hiện cũng đang đặt nghi vấn, có hay không sự móc ngoặc, bắt tay đi đêm của những cơ quan này với nhau.
“Việc này, theo tôi cũng cần các cơ quan chức năng vào cuộc điều tra làm rõ. Có thể từ vụ án này chúng ta tìm ra được nhiều manh mối khác để làm rõ một sự thật. Ai không có tội thì mình cũng cần phải rõ ràng, minh oan cho họ”, ông Nhưỡng bày tỏ.
Để siết chặt lỗ hổng quản lý tại một số địa phương ông Lưu Bình Nhưỡng cho rằng, trước hết phải siết chặt công tác lãnh đạo, chỉ đạo điều hành trong ngành y tế.
Từ đồng chí Bộ trưởng cũng phải quán triệt, rút kinh nghiệm, xử lý trong toàn ngành. Mình phải lấy từ trường hợp này làm điển hình để thực hiện chứ không thể xử lý đơn lẻ như trước. Ngoài ra, phải tiếp tục làm một đợt thanh tra mạnh, trên diện rộng trong toàn ngành y tế. Cần thiết có thể lập các đoàn giám sát của Quốc hội và Hội đồng nhân dân địa phương để tổ chức giám sát về vấn đề này.
Chuyên gia cho rằng, trong khi cả nước đang căng mình chống dịch, làm mọi việc nhân nghĩa để lo cho dân, thì Công ty Việt Á lại đi cấu kết với quan chức ở “cơ quan cần nhân đạo nhất (Y tế)” để trục lợi một cách vô nhân đạo trên nỗi đau của người dân như vậy là không thể chấp nhận được, cần phải xử lý nghiêm.
“Đây không chỉ là hành vi vô đạo đức mà còn là trái pháp luật. Các cơ quan điều tra đã vào cuộc và đưa sự việc này ra ánh sáng một cách kịp thời như vậy khiến người dân rất hoan nghênh. Nhưng sau sự việc này, không đơn giản chỉ là một, hai nhân vật mà sẽ còn rất nhiều “dây dợ” sẽ bị xử lý”, TS. Lưu Bình Nhưỡng khẳng định.
Ông Trần Ngọc Vinh, nguyên ĐBQH khóa XII, XIII cũng cho rằng, trong vụ việc của Việt Á, cần xác định được rõ công ty Việt Á thực sự là của ai.
“Trong việc này, đầu tiên chúng ta phải xác định, Công ty Việt Á là của ai, trực thuộc đơn vị nào? Nó làm ăn không minh bạch như thế mà tại sao lại có thể tồn lại bao nhiêu năm nay”, ông Vinh nói.
Theo ông Vinh, dư luận tin tưởng và trông chờ Bộ Công an mở rộng điều tra để trả lại sự hoạt động minh bạch cho thị trường cung cấp trang thiết bi, vật tư y tế. Cá nhân nào mắc sai phạm đến đâu thì xử lý đến đó. Sau sự việc này cũng cần ngành y tế rà soát kỹ về chất lượng, giá thành, xuất xứ của các sản phẩm kit khác trên thị trường xem đã đúng chưa. Đồng thời, xem xét kỹ lưỡng việc cho thực hiện đấu thầu, đấu giá của các công ty cung ứng để đảm bảo khách quan, chọn đúng đối tượng. Cần tránh việc tiếp diễn câu chuyện có tổ chức đấu giá nhưng đâu đó chỉ là hình thức.
Ông Trần Ngọc Vinh khẳng định, vụ án của Công ty Việt Á phải xử nghiêm, đặc biệt là trách nhiệm của người đứng đầu. Một số lượng lớn sản phẩm kit xét nghiệm được lưu hành và sử dụng trong địa phương mình quản lý lại nói không biết về giá cả của bộ kit đó như thế nào thì ai chấp nhận được, như vậy là vô trách nhiệm.
“Trong việc này chúng ta có thể nhận định rằng, nó có cả một đường dây, cả một hệ thống thì nó mới trót lọt, chứ không thể dễ dàng như thế”, ông Vinh đặt vấn đề.
TS. Lưu Bình Nhưỡng cũng cho rằng, vụ án của Công ty Việt Á phải xử đến cùng mọi ngóc ngách, để bóc trần sự việc.
“Thủ tướng cũng đã có chỉ đạo, phải xem xét những trường hợp vi phạm lần này phải đưa ra hết”, ông Lưu Bình Nhưỡng kiên quyết đề nghị